Đã đành rằng sự ức chế thoái hóa peptide ruột dẫn đến các chất ức chế DPP4 như một phương pháp mới của liệu pháp điều trị tiểu đường thì liệu việc tăng bài tiết peptide ruột cũng mở ra con đường trị liệu mới? Hơn nữa, sự kết hợp của cả hai phương pháp có thể cho phép thậm chí mạnh hơn về giảm glucose và giảm cân?
Nhiều thụ thể khác- đa số trong đó là các thụ thể gắn với G-protein -điều chỉnh bài tiết peptide ruột trong phản ứng với các chất dinh dưỡng như axit béo, axit amin, carbohydrate, và các kích thích khác. Tuy nhiên, mặc dù có một lượng lớn nỗ lực nghiên cứu dành cho các thụ thể này, phương pháp trị liệu cho đến nay vẫn khó nắm bắt.
1. Receptor cho axit mật
Ngoài việc hỗ trợ tiêu hóa chất béo và chất béo hòa tan trong thức ăn, axit mật kích hoạt thụ thể hoóc môn nhân tế bào FXR và thụ thể acid mật gắn với G-protein 1, phổ biến hơn gọi là TGR5. Trong khi việc kích hoạt FXR điều chỉnh tổng hợp axit mật và chuyển hóa chất béo trung tính, kích hoạt TGR5 dẫn đến việc sản xuất GLP-1 và PYY từ các tế bào L và tăng sử dụng năng lượng, ít nhất là ở chuột. Chất chủ vận FXR hiện đang được nghiên cứu để điều trị NASH với kết quả đầy hứa hẹn trong các nghiên cứu lâm sàng cho đến nay. Trong khi các nghiên cứu ban đầu với chất chủ vận TGR5, chẳng hạn như chất tương đồng axit mật INT-777, đã tạo ra tác dụng mạnh đối với bài tiết incretin và giải phóng glucose ở loài gặm nhấm tuy nhiên tác dụng phụ qua trung gian đích cho đến nay đã ngăn chặn việc đưa TGR5 tham gia đánh giá lâm sàng. Cụ thể, kích hoạt TGR5 dẫn đến thư giãn cơ trơn và kích thích làm đầy túi mật, dẫn đến tăng mạnh kích thước túi mật không thể tách khỏi việc tăng GLP-1 hoặc cân bằng nội môi glucose. Tăng giải trình của TGR5 trong túi mật là những nỗ lực hiện tại được tập trung vào giảm tiếp xúc hệ thống của chất chủ vận TGR5 bằng cách tạo hợp chất ức chế ruột.
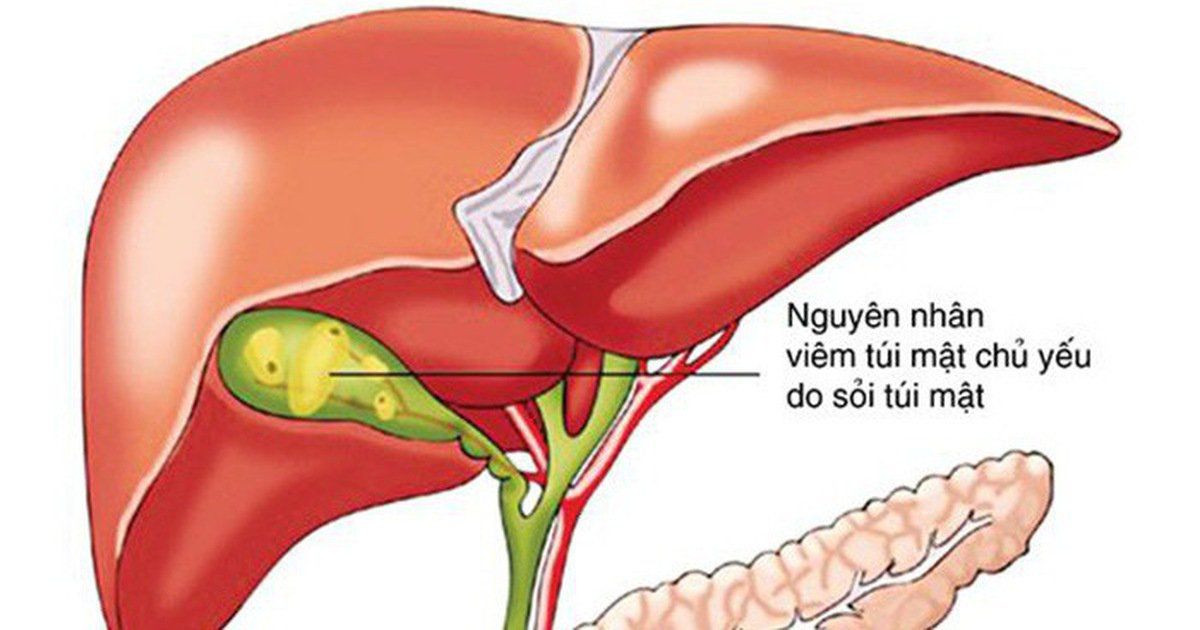
Tăng giải trình của TGR5 trong túi mật là những nỗ lực hiện tại được tập trung
2. Receptor cho axit béo mạch dài và liên quan Lipid
Các thụ thể gắn G-protein GPR40, GPR119 và GPR120 chia sẻ mối quan hệ với các axit béo chuỗi dài và có liên quan phân tử. Sự quan tâm đến GPR119 tăng đáng kể sau khi nó được xác định như một thụ thể điều hòa tác dụng ức chế của 2-monoacylglycerol, cụ thể là oleoylethanolamide, trên lượng thức ăn. Ngoài ra, GPR119 biểu hiện rất cao trong các tế bào enteroendocrine trong ruột cũng như trong đảo tụy. Rất nhiều chất chủ vận GPR119 mạnh và chọn lọc đã được xác định, và các nghiên cứu tiền lâm sàng cho thấy một hình ảnh nhất quán: các phân tử gây ra bài tiết insulin phụ thuộc glucose và tăng nhẹ bài tiết GLP-1 và GIP nhưng có ít hoặc không ảnh hưởng đến trọng lượng cơ thể. Nghiên cứu lâm sàng được thực hiện với nhiều hơn 10 phân tử. Trong khi giảm glucose đã được quan sát, hiệu ứng kích thích rất khiêm tốn, tác động đến mức GLP-1 và GIP là tối thiểu (<50%) và không thấy giảm cân đáng kể. Những tác động khiêm tốn này đã dẫn đến việc ngừng hoạt động phần lớn các nghiên cứu chất chủ vận GPR119.
Chất chủ vận GPR40 ban đầu được phát triển là chất tiết insulin phụ thuộc glucose và sau đó được phát hiện cũng có tiềm năng tiết GLP-1, phản ánh biểu hiện của thụ thể này trên các tế bào beta tuyến tụy cũng như tế bào enteroendocrine. Thuốc chủ vận GPR40 thế hệ thứ nhất, như fasiglifam (TAK-875), là chất chủ vận từng phần cho thấy hạ thấp glucose đáng kể trong phòng khám nhưng không tăng nồng độ GLP-1 cả cận lâm sàng và lâm sàng; không ảnh hưởng đến trọng lượng cơ thể đã được ghi nhận. Trong khi ngưng sử dụng fasiglifam là do lo ngại về tổn thương gan do thuốc, một số chất chủ vận GPR40 một phần vẫn còn trong nghiên cứu phát triển lâm sàng. Gần đây, các chất chủ vận đầy đủ của thụ thể GPR40 đã được phát triển liên kết với một trang web riêng biệt và kích hoạt cả tín hiệu Gaq và Gas. Trong các nghiên cứu tiền lâm sàng, các phân tử này là một trong những loại thuốc tiết insulin và incretin mạnh nhất được mô tả, dẫn đến tăng gấp 3 đến 5 lần trong nồng độ GLP-1 trong máu cũng như mức độ PYY và GIP tăng cao, và tăng mạnh bài tiết insulin phụ thuộc glucose. Tuy nhiên, mặc dù có những nỗ lực đáng kể, cho đến nay, chưa có chất chủ vận GPR40 đầy đủ nào bước vào thử nghiệm lâm sàng.
GPR120 là một thụ thể cho các axit béo chuỗi dài biểu hiện trong nhiều mô, nổi bật nhất là tế bào mỡ, tế bào miễn dịch, và tế bào enteroendocrine của ruột. Nhiều công ty như cũng như các nhà điều tra học thuật đã phát triển nhỏ các chất chủ vận GPR120 phân tử và chứng minh tác dụng hạ glucose ở loài gặm nhấm trong môi trường cấp tính và mãn tính. Tuy nhiên, bài tiết GLP-1 chỉ được báo cáo ở một vài phân tử có kết quả hỗn hợp và sự phát triển các phân tử tác động chọn lọc GPR120 vẫn còn là thách thức . Đến nay vẫn chưa có nghiên cứu lâm sàng với chất chủ vận GPR120 được công bố.
3. Receptor cho axit amin
Một thụ thể dinh dưỡng tương đối gần đây sẽ được khám phá là GPR142, bây giờ được công nhận là một thụ thể cho các axit amin thơm điều hòa bài tiết incretin từ ruột, cũng như glucagon và bài tiết insulin từ các đảo tụy. Các chất chủ vận chọn lọc GPR142 phân tử nhỏ gây tăng bài tiết insulin và glucagon từ chuột và đảo tụy người; cải thiện dung nạp glucose đường uống khi dùng thuốc cấp tính ở chuột gầy và béo phì, cũng như ở khỉ; và cải thiện độ nhạy insulin và mức glucose cơ bản khi gây chuột béo phì do chế độ ăn kiêng. Các peptide ruột trong tuần hoàn, bao gồm GLP-1, GIP và CCK tăng đáng kể ở cả loài gặm nhấm và không phải người linh trưởng với chất chủ vận GPR142 đặc biệt mạnh (5 lần) có hiệu lực trên GIP. Thật thú vị, chất chủ vận GPR142 có thể gây ra cả sự tăng sinh tế bào beta cũng như bảo vệ các tế bào beta khỏi stress ở các đảo tụy bị cô lập trong ống nghiệm, cho thấy tiềm năng tăng độ bền của trị liệu. Cho đến nay, không có nghiên cứu lâm sàng nào với chất chủ vận GPR142 được báo cáo.
.png)









