1. Vai trò các xét nghiệm máu
- Kháng thể kháng tế bào thành: Việc tìm ra các kháng thể đặc hiệu trong VDDTM giúp sàng lọc và khẳng định chẩn đoán hữu hiệu hơn. Các kháng thể được sử dụng nhiều nhất là kháng thể kháng tế bào thành (anti-parietal cell antibody-APCA).
- Kháng thể kháng yếu tố nội tại. Theo một nghiên cứu kháng thể kháng tế bào thành độ nhạy và độ đặc hiệu lần lượt 81%, 90%, trong khi kháng yếu tố nội tại có độ đặc hiệu 100% nhưng độ nhạy kém 27%.
- Định lượng nồng độ gastrin 17 cũng giúp đánh giá tình trạng tăng bài tiết gastrin từ tế bào G do giảm sự bài tiết dịch vị. Chẩn đoán bằng việc phối hợp các xét nghiệm kháng thể kháng tế bào thành, kháng yếu tố nội, gastrin 17, kết quả giải phẫu bệnh. Tăng nồng độ gastrin còn có thể gặp trong một số bệnh lý khác như hội chứng Zollinger Ellison vì vậy để chẩn đoán phân biệt có thể tiến hành đo nồng độ acid sản xuất ra trong dạ dày. Ở bệnh nhân viêm teo dạ dày mạn tính, nồng độ acid dịch vị sản xuất ra thấp < 5mEg/giờ trong khi ở bệnh nhân mắc Zollinger Ellison, nồng độ này 10 mEg/giờ. Ngoài ra cần loại trừ các trường hợp có tắc nghẽn hoặc rối loạn nhu động ở dạ dày bằng nội soi và các phương pháp thăm dò khác.
- Pepsinnogen (PG) I, II: Việc đo nồng độ và sử dụng chỉ số PGI/PGII để phối hợp chẩn đoán. PGI được sản xuất bởi các tế bào chính của vùng niêm mạc thân phình vị dạ dày trong khi PGII sản xuất bởi cả tế bào chính và tế bào cổ tuyến ở toàn bộ niêm mạc dạ dày. Do vậy trong viêm dạ dày tự miễn sẽ có giảm nồng độ PGI và chỉ số PGI/PGII <3.
- Bệnh nhân thiếu máu hồng cầu to nên định lượng vitamin B12, homocystein và acid methylmalonic. Giá trị của chúng này có thể thay đổi theo thời gian tuy nhiên một số trường hợp các giá trị vẫn trong giới hạn bình thường.
- Sắt huyết thanh: giúp đánh giá toàn diện về vấn đề thiếu máu của người bệnh.
Mỗi một xét nghiệm máu đều có vai trò nhất định
Đánh giá về mặt đại thể chủ yếu dựa vào các mẫu bệnh phẩm khi cắt dạ dày. Ở giai đoạn đầu không có nhiều sự biến đổi rõ rệt ở niêm mạc nhưng khi tình trạng viêm teo tiến triển niêm mạc thân vị trở nên mỏng hơn, các nếp niêm mạc bị dẹt đi. Ngoài ra có thể thấy những nốt nhỏ (polyp tăng sản, giả polyp, polyp dạng adenoma, u carcinoid...).
Về mặt vi thể viêm dạ dày tự miễn được tổn thương viêm teo tập trung khu trú ở thân vị với các hình ảnh dị sản ruột, dị sản tế bào nang tuyến tụy hoặc tăng sản các tế bào ưa crôm. Khi không có tình trạng đồng nhiễm HP niêm mạc hang vị bình thường hoặc chỉ là hình ảnh viêm phản ứng nhẹ.
Có thể chia các biến đổi trên tổn thương vi thể ra làm ba giai đoạn:
- Giai đoạn sớm: đặc trưng bởi sự xâm nhập của các tế bào lympho và tương bào vào niêm mạc vùng bài tiết acid làm tăng chiều dày lớp màng đáy. Quá trình này có thể có sự tham gia của cả các tế bào ưa acid và dưỡng bào. Ngoài ra, bắt đầu quan sát thấy sự phá hủy các tuyến bài tiết acid dịch vị bởi các tế bào lympho xảy ra ở từng vùng. Những đặc điểm trong giai đoạn sớm này thường không đặc hiệu do vậy các nhà giải phẫu bệnh có thể mới chỉ nghi ngờ và đề nghị phối hợp thêm với các xét nghiệm huyết thanh tìm kháng thể kháng tế bào thành và kháng thể kháng yếu tố nội.
- Ở giai đoạn thứ hai: có sự xâm nhập của các tế bào lympho, tương bào mạnh mẽ hơn, thấy rõ hiện tượng viêm teo của các tuyến bài tiết acid, độ dày của lớp niêm mạc thường không thay đổi hoặc đôi khi bị giảm đi. Có thể quan sát rõ các hình ảnh dị sản ruột hoặc dị sản giả môn vị. Trong giai đoạn này nếu chỉ thấy tổn thương viêm teo rõ ở mảnh sinh thiết thân vị trong khi mảnh sinh thiết từ hang vị bình thường, các nhà giải phẫu bệnh có thể khẳng định chẩn đoán VDDTM.
Giai đoạn cuối được đặc trưng bởi tình trạng giảm nhiều hoặc mất hẳn các tuyến bài tiết acid dịch vị, có thể thấy hình thành các polyp tăng sản hoặc polyp viêm. Dị sản giả môn vị, dị sản ruột, dị sản tế bào tuyến nang của tụy lan rộng và có thể thấy lớp cơ niêm dày lên. Đôi khi có thể thấy tổn thương tăng sản của các tế bào ECL. Sử dụng các chất hóa mô miễn dịch sẽ giúp việc chẩn đoán dễ dàng hơn.
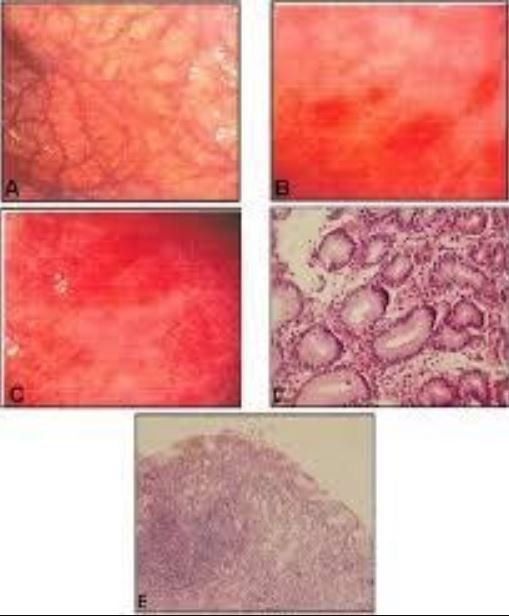
Hình ảnh mô bệnh học của viêm teo dạ dày
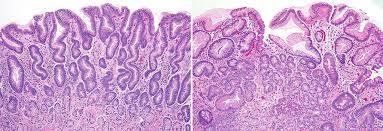
Hình ảnh viêm dạ dày tự miễn (hình bên phải) với mất các cấu trúc ống tuyến, so với hình bên trái các câu trúc tuyến còn bình thường
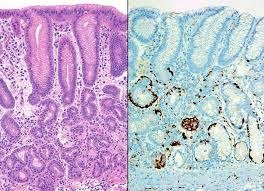
Viêm dạ dày tự miễn được xác định thêm bằng phương pháp nhuộm hóa mô miễn dịch.
Tài liệu tham khảo
- Đào Việt Hằng-Đào Văn Long(2018), “Viêm dạ dày tự miễn”, Bệnh lý tự miễn –dị ứng đường tiêu hóa, Nhà sản xuất y học.
- Carmel R(2996) Prevalence of undiagnosed pernicious anemia in the elderty Arch Intern Med, 156 1097-200.
3. Andres E, Serraj K (2012), Optimal management of pernicious anemia. JBlood Med, 3:97-103.
4. S Strickland RG, Mackay IR (1973), A reappraisal of the nature and significance of chronic atrophic gastritis. Am J Dig Dis, 18:426-40.
5. Park JY, Lam-Himlin D, Vemulapalli R (2013). Review of autoimmune metaplastic atrophic gastritis. Gastrointest Endosc, 77(2):284-92.
6. Kulnigg-Dabsch S.(2016), “Autoimmune gastritis”, Wien Med Wochenschr 166(13-14):424-430
.png)









